Первичной структурой называют порядок чередования (последовательность) аминокислотных остатков в белке. Даже идентичные по длине и аминокислотному составу пептиды могут быть разными веществами. Например, из двух аминокислот — аланина и тирозина — можно построить два пептида: Ala—Туг и Туг—Ala. Из трех аминокислот можно получить шесть различных по первичной структуре трипептидов.
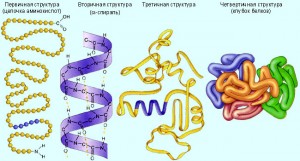
- Структуры белков.
Читать дальше »
Длинные полипептидные цепи (длиной около 200 аминокислотных остатков или больше) обычно имеют доменную пространственную структуру. Доменом называют часть пептидной цепи, образующей как бы самостоятельную глобулу, причем на одной пептидной цепи может быть два или больше доменов.
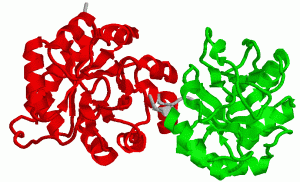
- Доменная структура.
Читать дальше »
Белок, выполняющий определенную функцию в живой клетке, может быть представлен несколькими формами — изофункциональными белками, или изобелка-ми. Например, в эритроцитах человека обнаружено несколько форм гемоглобина: у взрослого человека преобладающими формами являются НЬА, на долю которого приходится 96 % всего гемоглобина, HbF и НЬА^ (примерно по 2 % каждого).
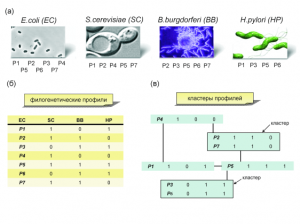
- Изофункциональный белок.
Читать дальше »
Скорость реакции чаще всего определяется ее энергией активации, т. е. той энергией, которую нужно сообщить молекулам, чтобы началось химическое превращение.
Чем больше энергия активации, тем меньше скорость реакции. Энергия активации зависит от природы реагирующих молекул, от их внутреннего строения. Например, энергия активации реакции S02 с кислородом больше, чем энергия активации реакции S02 с N02.
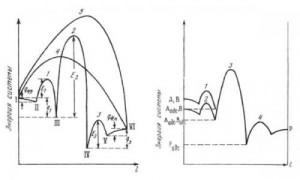
- Энергия активации реакций.
Читать дальше »
Наиболее характерная черта, отличающая ферменты от других катализаторов — высокая специфичность их действия. Активный центр ферментов, как и других белков, образован боковыми группами аминокислотных остатков пептидной цепи. Строение активных центров ферментов, катализирующих разные реакции, различно.

- Действие ферментов.
Читать дальше »
Многие ферменты для проявления каталитической активности нуждаются в присутствии некоторых веществ непептидной природы — кофакторов. Различают две группы кофакторов: ионы металлов (а также некоторые неорганические анионы) и коферменты, которые представляют собой органические вещества.Примерно треть всех известных ферментов содержит ион металла или активируется ионами металла.
- Кофактор ферментов.
Читать дальше »
Молекула кофермента А построена из аденозин-3'-фосфат-5'-пирофосфата, соединенного сложноэфирной связью с пантотеновой кислотой, которая, в свою очередь, соединена амидной связью с р-меркаптоэтиламином (тиоэтаноламином).
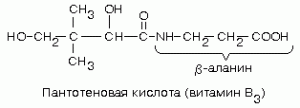
- Кофермент.
Читать дальше »
Метаболизмом называют химические превращения веществ в организме (от греч. metabole — изменение, превращение). Вещества, участвующие в метаболизме, называют метаболитами. Метаболизм — результат действия ферментов: все реакции, определяющие баланс веществ в живой клетке, катализируются ферментами.
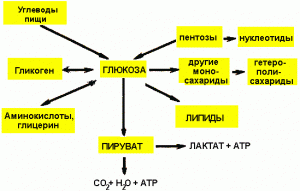
- Метаболизм глюкозы.
Читать дальше »
Многие ферменты могут обратимо связывать определенные метаболиты, ингиби-рующие или активирующие фермент. Такие метаболиты называют эффекторами.
Эффектор присоединяется не к каталитическому активному центру фермента, а к специальному регуляторному центру, который называют также аллостеричес-ким центром («в другом месте расположенный центр»).
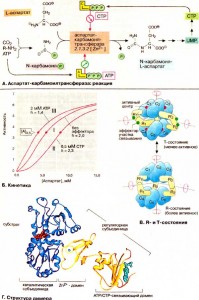
- Пример аллостерической регуляции.
Читать дальше »
Протеинкиназы катализируют фосфорилирование белков по гидроксильным группам серина, треонина и тирозина. Если фосфорилируемые белки это тоже ферменты, то их активность в результате фосфорилирования в одних случаях уменьшается, в других — увеличивается. Например, в клетках жировой ткани есть липаза, существующая в двух формах — фосфопротеина и простого белка.
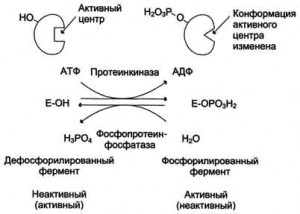
- Регуляция ферментов.
Читать дальше »














