Первоначальные этапы истории биохимии совпадают с историей органической химии. До середины XIX в. органической химией называли науку, которая изучала вещества, входящие в состав животных и растительных организмов, т. е. вещества живого («органического») мира. Позднее, в связи с развитием синтетической химии соединений углерода, смысл термина «органическая химия» изменился — так теперь называют химию соединений углерода, а науку, изучающую химический состав живых организмов и химические процессы, протекающие в них, стали называть физиологической, а затем биологической химией.
- Первоначальные этапы.
Читать дальше »
Представление о белках как о классе соединений формировалось в XVIII-XIX вв. В этот период из разнообразных объектов живого мира (семена и соки растений, мышцы, хрусталик глаза, кровь, молоко и т. п.) были выделены вещества, обладающие сходными свойствами: они образовывали вязкие, клейкие растворы, свертывались при нагревании, при их высушивании получалась роговидная масса, при «анализе огнем» ощущался запах паленой шерсти или рога и выделялся аммиак.
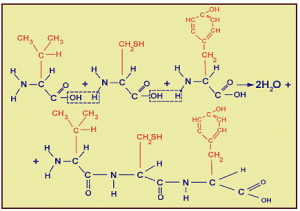
- Белки как класс соединений.
Читать дальше »
Даже при одинаковой длине пептиды являются разными веществами, если они различаются по аминокислотному составу.В первом из них есть остатки лизина, глицина и серина, которых нет во втором. В то же время во втором есть остатки изолейцина, аспарагиновой кислоты и тирозина, которых нет в первом.
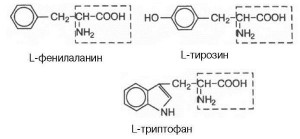
- Аминокислотный состав белков.
Читать дальше »
Первичной структурой называют порядок чередования (последовательность) аминокислотных остатков в белке. Даже идентичные по длине и аминокислотному составу пептиды могут быть разными веществами. Например, из двух аминокислот — аланина и тирозина — можно построить два пептида: Ala—Туг и Туг—Ala. Из трех аминокислот можно получить шесть различных по первичной структуре трипептидов.
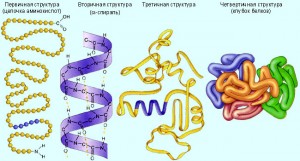
- Структуры белков.
Читать дальше »
Пептидная цепь обладает значительной гибкостью. В результате внутрицепочеч-ных взаимодействий она приобретает определенную пространственную структуру (конформацию). Основным методом изучения трехмерной структуры белков служит рентгеноструктурный анализ. Он основан на дифракции и интерференции рентгеновских лучей, проходящих через кристалл изучаемого вещества.
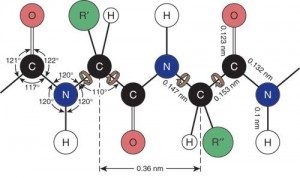
- Пептидная цепь.
Читать дальше »
При разрыве большого числа связей, стабилизирующих пространственную структуру белковой молекулы, упорядоченная, уникальная для каждого белка конформация пептидной цепи нарушается, и молекула целиком или в значительной части принимает форму случайного беспорядочного клубка (случайного в том смысле, что каждая молекула данного индивидуального белка по конформации может отличаться от всех других молекул).
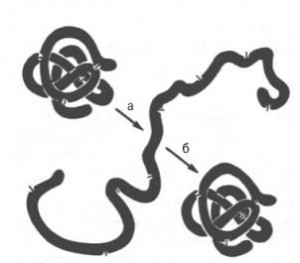
- Денатурация.
Читать дальше »
Характерная структурная особенность фибриллярных белков — вытянутая, нитевидная форма молекул. Эти белки нерастворимы в воде и часто образуют многомолекулярные нитевидные комплексы — фибриллы.
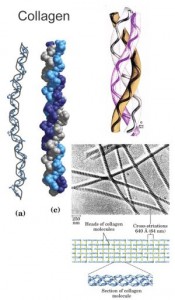
- Фибриллярный белок.
Читать дальше »
Хотя взаимодействие белка с его физиологическим лигандом отличается высокой специфичностью, всегда можно подобрать вещество, природное или синтетическое, которое является структурным аналогом лиганда и тоже комплементарно центру связывания. Если такой аналог ввести в организм, то он будет соединяться с соответствующим белком вместо естественного лиганда, в результате чего функция белка окажется заблокированной.

- Исследование функций белков.
Читать дальше »
Процедура выделения какого-либо белка начинается с переведения белков ткани в раствор. Для этого ткань измельчают и клетки разрушают с помощью специальных приборов — гомогенизаторов, или просто растиранием с песком. Нерастворимые части ткани из гомогената осаждают центрифугированием. В надосадочной жидкости (экстракте) содержатся растворимые белки.
- Процедура выделения белка.
Читать дальше »
История изучения ферментов тесно переплетается с историей изучения катализа вообще. Напомним, что катализом называют ускорение химической реакции, вызванное добавлением малых, нестехиометрических количеств определенного вещества — катализатора. Например, платина ускоряет разложение пероксида водорода на кислород и воду, кислоты ускоряют разложение белков на аминокислоты, крахмала на глюкозу, мочевины на С02 и NH3, и т. д.
- Катализ.
Читать дальше »














